iPSC技术简介
诱导多能干细胞(iPSC)技术背景知识
诱导多能干细胞(iPSC,Induced Pluripotent Stem Cells)技术是由日本科学家山中伸弥教授于2006年首次提出的一项突破性研究成果。该技术通过将体细胞重新编程为具有多能性(pluripotency)的状态,从而使这些细胞能够分化成多种类型的细胞。与传统的胚胎干细胞(ESC)相比,iPSC技术的出现不仅避免了伦理问题,还为再生医学、药物筛选和疾病建模等方面开辟了新的研究和应用领域。本文将详细介绍iPSC技术的背景、原理、优势、挑战以及在眼科和神经领域的应用进展。
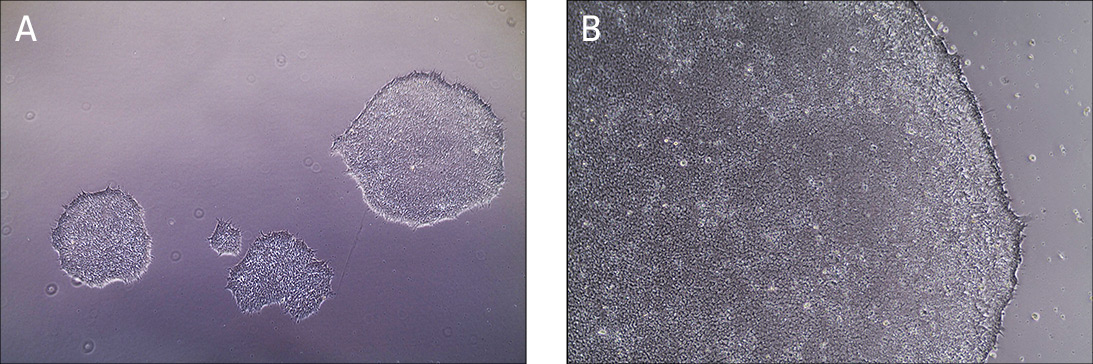
iPSC细胞的形态
iPSC技术的起源与发展
在iPSC技术提出之前,胚胎干细胞(ESC)是唯一已知的多能干细胞来源。ESC能够分化为三种胚层的所有细胞类型,因此具有极大的临床应用潜力。然而,ESC的获取通常需要从胚胎中提取,这一过程引发了广泛的伦理争议。iPSC的发明解决了这一伦理难题,因为iPSC来源于成年体细胞(如皮肤细胞或血液细胞),因此不依赖于胚胎。
山中伸弥及其团队的研究表明,通过转入4个转录因子(Oct4、Sox2、Klf4和c-Myc,统称为OSKM),可以将已分化的成体细胞重新编程为具有胚胎干细胞特征的多能性细胞。iPSC与ESC具有相似的多能性,能够分化为体内所有类型的细胞。因此,iPSC不仅为干细胞研究提供了新的思路,也为临床治疗提供了潜在的细胞治疗资源。
iPSC技术的原理
iPSC的生成基于细胞重编程的过程。重编程是指通过外源性因子改变细胞的基因表达谱,使其恢复到多能状态。山中伸弥和他的团队发现,Oct4、Sox2、Klf4和c-Myc四个转录因子对细胞重编程至关重要。这些转录因子在胚胎发育过程中发挥着重要作用,能够激活胚胎干细胞的基因表达并抑制分化相关基因的表达。通过这些因子的共同作用,成熟体细胞可以被转化为具有胚胎干细胞性质的iPSC。
iPSC的多能性表现为其能在适当条件下分化为三胚层(外胚层、中胚层、内胚层)的任何类型细胞,包括心脏、神经、肌肉和肝脏等不同组织的细胞。因此,iPSC在基础研究、疾病建模、药物筛选和再生医学等方面都有着重要的应用价值。
iPSC的优势
iPSC技术有以下几个重要优势:
避免伦理问题:与传统的胚胎干细胞相比,iPSC来源于成人体细胞,因此可以避免从胚胎中获取细胞所涉及的伦理问题。
个性化医疗:iPSC能够从患者自体细胞中获得,因此可以制作个体化的细胞模型,用于精准医学和个性化治疗。这使得iPSC成为治疗一些遗传性疾病的潜在途径。
疾病模型与药物筛选:利用iPSC技术,可以在实验室内生成各种疾病模型,帮助科学家研究疾病的发生机制以及药物的作用。例如,针对神经退行性疾病、心血管疾病等,iPSC可以提供非常有效的体外模型。
再生医学:iPSC具有广泛的分化潜力,因此可以为再生医学提供潜在的治疗资源。研究者已在实验室中成功将iPSC分化为多种体细胞,如神经细胞、心脏细胞和视网膜细胞,这为相关疾病的细胞治疗提供了新的希望。
iPSC细胞示意
iPSC技术面临的挑战
尽管iPSC技术具有巨大的潜力,但也面临许多挑战:
低效的重编程过程:尽管iPSC的技术已取得了显著进展,但目前iPSC的重编程效率仍然较低,且需要较长的时间。这在实际应用中可能会成为限制因素。
基因组不稳定性:iPSC技术中使用的转录因子(如c-Myc)可能引发基因组的不稳定性,增加了肿瘤发生的风险。因此,如何提高iPSC的基因安全性是当前研究的重点之一。
分化和成熟问题:虽然iPSC能够分化为不同类型的细胞,但这些分化后的细胞往往尚未完全成熟,功能可能不完全。因此,如何改善iPSC分化后细胞的功能和稳定性,仍然是一个亟待解决的问题。
免疫排斥问题:虽然自体iPSC能有效避免免疫排斥反应,但在一些情况下,由于iPSC的重编程过程中可能存在突变,仍然可能引发免疫反应。因此,如何确保iPSC治疗的长期安全性仍然是一个需要关注的问题。
iPSC技术在各个领域的应用
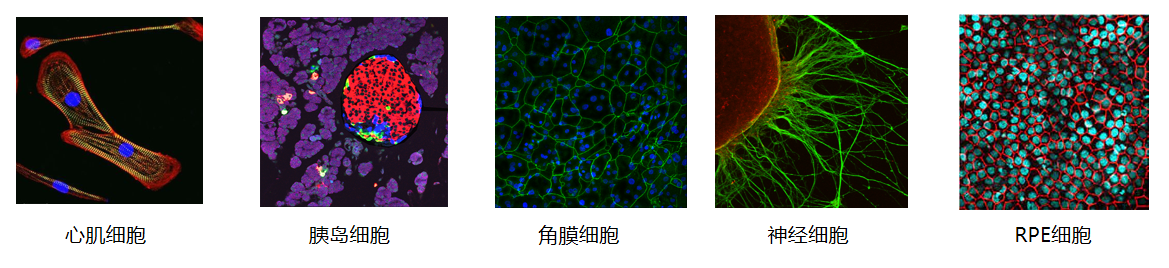
1. 心肌细胞的分化
心肌细胞的分化是iPSC技术应用中的又一个重要领域。通过控制特定的诱导条件,iPSC可以成功分化为功能性的心肌细胞,包括心脏收缩功能和电生理活动的表现。这些iPSC衍生的心肌细胞在心脏疾病的研究中具有重要应用价值。例如,它们被用来研究心脏疾病的发生机制、筛选抗心脏病药物,并为心脏病患者提供可能的再生治疗方案。由于iPSC来源于患者自身,减少了免疫排斥反应,因此为心脏疾病的个性化治疗提供了新的思路。
2. 肝细胞和胰岛细胞的分化
iPSC的分化还涉及到内脏细胞的生成,如肝细胞和胰岛β细胞。通过细胞培养条件的优化,iPSC可以分化为具有生理功能的肝细胞,这些肝细胞可用于肝病的研究以及药物毒性测试。而胰岛β细胞的生成则为糖尿病的研究和治疗提供了新的方向。特别是在1型糖尿病的治疗中,通过将iPSC分化为胰岛β细胞,并将这些细胞移植到糖尿病患者体内,可能为治疗提供新的希望。
3. 血液细胞的分化
iPSC还可以分化为各种血液细胞,包括红细胞、白细胞和血小板等。通过定向分化,iPSC能生成功能性血液细胞,这在造血系统疾病(如白血病和贫血)中有着广泛的应用前景。iPSC衍生的血液细胞不仅可用于疾病模型的构建,还可用于研究血液系统的发育过程,甚至为血液病患者提供可能的细胞治疗方案。
4. 眼科领域的应用
iPSC技术在眼科和神经领域的临床应用潜力巨大,尤其在视网膜退行性疾病和神经退行性疾病的治疗方面展现了广阔的前景。
眼科领域中,iPSC技术的应用主要集中在视网膜疾病的治疗。视网膜黄斑变性、视网膜色素变性等眼科疾病常常导致不可逆的视力丧失,且目前的治疗手段有限,因此,iPSC提供了潜在的治疗方案。研究人员通过将iPSC分化为视网膜色素上皮细胞(RPE细胞)或视网膜神经节细胞,试图恢复视力。2015年,日本团队成功将iPSC分化为视网膜色素上皮细胞,并将这些细胞移植到患有视网膜色素变性患者体内,取得了初步的临床试验成功。此外,iPSC技术还被用于开发视网膜疾病的个性化模型,用于药物筛选和毒性测试。尽管这些研究仍处于早期阶段,但iPSC的临床转化应用为视网膜疾病治疗带来了新的希望。
iPSC-RPE(视网膜色素上皮细胞)
5. 神经领域的应用
在神经领域,iPSC技术已被广泛应用于神经退行性疾病,如帕金森病、阿尔茨海默病、脊髓损伤等的研究和治疗。在帕金森病方面,研究人员已通过将患者的体细胞转化为iPSC,并进一步将其分化为多巴胺能神经元,来探索细胞替代治疗的可能性。2019年,全球首个基于iPSC的帕金森病临床试验在日本开展,研究者通过移植患者自身的iPSC衍生的多巴胺能神经元来恢复运动功能。尽管该试验仍处于早期阶段,但其初步结果为iPSC技术在神经退行性疾病中的应用提供了宝贵的临床数据。
此外,iPSC还被用于阿尔茨海默病和脊髓损伤的研究。通过建立患者特异性的iPSC模型,研究人员能够更好地理解疾病的机制,并为未来的治疗方案提供依据。
结论
iPSC技术自其诞生以来,已在基础医学研究、药物开发、疾病建模以及再生医学领域取得了显著进展。在眼科和神经领域,iPSC的应用前景尤其广阔,虽然目前仍面临一些技术性挑战,但随着研究的深入,iPSC技术有望成为治疗各类眼科和神经退行性疾病的关键工具。